Czym różni się Uran-235 od Uranu-238?
Kompleksowy przewodnik po izotopach uranu
I. Wstęp: Uran w sercu historii
Spacerując chłodnymi, wilgotnymi korytarzami dawnych kopalni w Kowarach, zwiedzający podążają śladami jednej z największych tajemnic powojennej Polski. To tutaj, pod przykrywką wydobycia fluorytu i barytu, Radziecko-Polska Spółka Akcyjna „Zakłady R-1” gorączkowo wydobywała surowiec, który miał odmienić bieg historii – uran. Materiał ten stał się kluczem do panowania nad światem, paliwem dla elektrowni i rdzeniem broni atomowej.
Jednak cała ta globalna strategia, cała presja polityczna i cały wysiłek górników Kowar sprowadza się do subtelnej, niemal niewidzialnej różnicy, tkwiącej w sercu każdego atomu: różnicy między Uranem-235 a Uranem-238. Oba są chemicznie identyczne, ale ich fizyczne właściwości sprawiają, że jeden jest bezcennym paliwem, a drugi jego obfitym, ale nieaktywnym bratem. Zrozumienie tej drobnej, trzy-neutronowej różnicy jest kluczem do rozszyfrowania historii Kowar i całej energetyki jądrowej.
W tym artykule dogłębnie zbadamy fizykę, geologię i strategiczne znaczenie tych dwóch izotopów, wyjaśniając, dlaczego tak mała zmiana w masie atomowej miała tak ogromne konsekwencje dla XX i XXI wieku.
II. Podstawy fizyki jądrowej: Czym jest izotop?
Aby zrozumieć uran, musimy zacząć od podstaw. Każdy atom składa się z jądra (zawierającego protony i neutrony) oraz krążących wokół niego elektronów. Liczba protonów w jądrze definiuje, z jakim pierwiastkiem chemicznym mamy do czynienia. Uran, niezależnie od izotopu, zawsze posiada 92 protony. To one nadają mu chemiczną tożsamość.
Izotopy to atomy tego samego pierwiastka, które różnią się wyłącznie liczbą neutronów. Ta różnica w masie, choć niewielka, jest fundamentalna.
| Izotop | Liczba Protonów | Liczba Neutronów | Liczba Masowa (A) | Występowanie (w %) |
| Uran-238 | 92 | 146 | 238 | ok. 99,274 % |
| Uran-235 | 92 | 143 | 235 | ok. 0,72 % |
| Uran-234 | 92 | 142 | 234 | ok. 0,006 % |
Jak widać, U-238 ma o trzy neutrony więcej niż U-235. To właśnie ta niewielka różnica w masie atomowej decyduje o tym, który izotop jest łatwopalnym „paliwem”, a który jest stabilnym „regulatorem”. Cała technologia jądrowa opiera się na separacji tych dwóch, niemal identycznych atomów.
III. Uran w wrzyrodzie: Tajemnica niskiej koncentracji
Skąd bierze się ten uran – ten niezwykły metal? Cała historia zaczyna się w kopalni uranu. To tam wydobywa się rudę zawierającą cenne izotopy. Problem leży w proporcjach: kopalnia uranu dostarczała materiał, w którym jeden izotop dominował nad drugim, tworząc potężną przeszkodę
Rudy uranu, takie jak blenda uranowa, wydobywana w Kowarach, są zdominowane przez U-238. Ten izotop stanowi absolutną większość uranu naturalnego, sięgającą 99,274%. Jest on niezwykle stabilny; jego okres półrozpadu wynosi około 4,5 miliarda lat – co jest niemal równe wiekowi Ziemi. Jego dominacja wynika właśnie z tej niesamowitej trwałości.
U-235 ma znacznie krótszy okres półrozpadu, wynoszący około 700 milionów lat. Oznacza to, że od momentu powstania Ziemi większość początkowej ilości U-235 już się rozpadła. Dziś, w każdej tonie wydobytej rudy, zaledwie 7 kilogramów to poszukiwany U-235.
To właśnie ta dramatycznie niska koncentracja stanowiła największe wyzwanie dla ZSRR. Radzieccy naukowcy i inżynierowie wiedzieli, że muszą zdobyć jak największą ilość tego cennego 0,72% surowca, aby uruchomić swój program nuklearny. Ta garstka cennego izotopu była celem całej tajnej i intensywnej eksploatacji Zakładów R-1.
Co więcej, U-238 jest źródłem naturalnego promieniowania tła. W miarę jego rozpadu powstaje cała kaskada produktów, z których najsłynniejszym jest Radon-222. To gaz promieniotwórczy, który naturalnie ulatnia się ze skał i gleby – stąd jego obecność w kopalniach. Ironią losu jest fakt, że w latach 70. i 80. w Kowarach urządzono Inhalatorium Radonowe, wierząc w leczniczą moc kontrolowanej ekspozycji na ten gaz, który był produktem rozpadu dominującego U-238.
IV. Kluczowa różnica fizyczna: Rozszczepienie
Najważniejsza i najbardziej strategiczna różnica między izotopami polega na ich reakcji na neutrony, a co za tym idzie – na ich zdolności do ulegania rozszczepieniu (fisji) jądrowej.
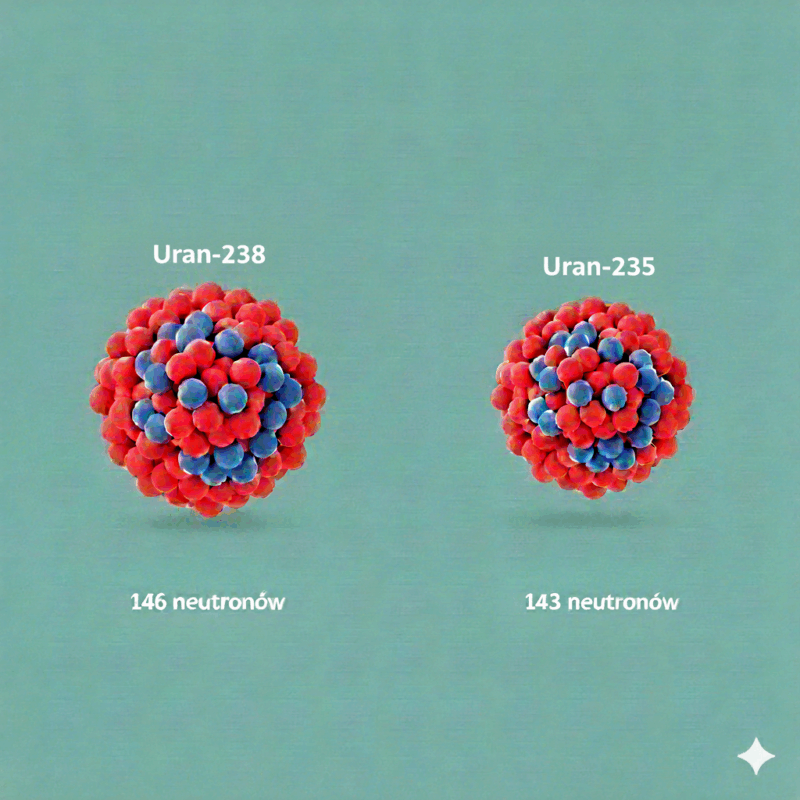
Na naszym obrazku widzimy modele jąder atomowych dwóch kluczowych izotopów uranu: Uranu-238 (po lewej, z 146 neutronami) oraz Uranu-235 (po prawej, z 143 neutronami). Ta niewielka różnica w liczbie neutronów ma fundamentalne znaczenie.
Uran-235: Katalizator reakcji łańcuchowej
U-235 jest izotopem rozszczepialnym (fissile). Jego jądro jest niestabilne i może zostać rozszczepione przez wolne, powolne (termiczne) neutrony, nawet te o bardzo małej energii kinetycznej.
Kiedy wolny neutron uderza w jądro U-235, pochłania je, a powstałe jądro jest tak niestabilne, że natychmiast rozpada się na dwa mniejsze jądra (produkty rozszczepienia), uwalniając przy tym ogromną ilość energii oraz – co kluczowe – średnio od 2 do 3 nowych neutronów. Te nowe neutrony mogą uderzyć w kolejne jądra U-235, podtrzymując tym samym samopodtrzymującą się reakcję łańcuchową.
To właśnie ta zdolność U-235 do podtrzymywania reakcji łańcuchowej czyni go paliwem. Bez tego procesu nie byłoby ani kontrolowanej mocy reaktora, ani potężnej eksplozji broni jądrowej.
Uran-238: Regulator i fabryka plutonu
U-238 jest izotopem płodnym (fertile). Nie jest w stanie podtrzymać reakcji łańcuchowej. Jego jądro może ulec rozszczepieniu tylko przez szybkie neutrony, ale pochłania wolne neutrony, nie rozszczepiając się.
W reaktorach U-238 odgrywa rolę pochłaniacza i regulatora, pomagając kontrolować przebieg reakcji. Jednak jego najważniejszą rolą jest przekształcenie się w inny cenny materiał. Kiedy U-238 pochłonie neutron, ulega dwóm szybkim rozpadom beta, przekształcając się w Pluton-239.
Pluton-239 jest sam w sobie izotopem rozszczepialnym i jest używany jako paliwo w reaktorach powielających oraz jako rdzeń w nowoczesnej broni jądrowej.
Dr John C. Harsanyi, fizyk jądrowy z Los Alamos National Laboratory, USA, podsumował to następująco:
„Uran-238 jest geologicznie stabilną kotwicą, która zapewnia nam zasoby na miliardy lat. Ale to Uran-235 jest wirtuozem, który potrafi zamienić pojedynczy neutron w lawinę energii. Bez tej różnicy, energia jądrowa pozostałaby tylko teorią.”
V. Wzbogacanie: Strategiczny most między skałą a bombą
Ponieważ uran wydobywany w Kowarach zawierał zaledwie 0,72% U-235, aby móc zasilić reaktor lub stworzyć bombę, konieczne było przeprowadzenie niezwykle kosztownego i skomplikowanego procesu: wzbogacania.
Wzbogacanie to proces fizycznego zwiększania koncentracji U-235 w stosunku do U-238. Z powodu ich identyczności chemicznej, oddzielanie izotopów jest wyzwaniem inżynieryjnym na najwyższym poziomie.
Poziomy wzbogacenia i Ich zastosowanie:
- Uran Naturalny (0,72% U-235): Taki uran jest używany tylko w specyficznych typach reaktorów (np. CANDU), które wykorzystują ciężką wodę jako moderator.
- Nisko Wzbogacony Uran (LEU: 3% – 5% U-235): To standardowe paliwo dla większości współczesnych reaktorów energetycznych na świecie (reaktory PWR/BWR).
- Wysoko Wzbogacony Uran (HEU: powyżej 20% U-235, do 90%+): Jest to materiał używany do napędów okrętów podwodnych i, co najważniejsze, do broni jądrowej (jak w bombie zrzuconej na Hiroszimę).
Metody separacji
Proces ten wymaga wykorzystania minimalnej różnicy masy atomowej:
- Dyfuzja Gazowa: Stosowana historycznie (np. w Projekcie Manhattan). Proces polegał na przepuszczaniu gazowego związku uranu (sześciofluorku uranu – UF_6) przez porowate membrany. Lżejszy U-235 dyfunduje nieco szybciej, co pozwala na stopniową, wieloetapową separację.
- Ultracentryfugi: Współczesna i energooszczędna metoda. W wirujących z ogromną prędkością cylindrach, siła odśrodkowa nieznacznie separuje cięższy U-238 na zewnątrz od lżejszego U-235, co pozwala na wydzielenie cennego izotopu.
Prof. Dr. Stanisław P. Woźnicki, specjalista ds. energetyki jądrowej z Politechniki Warszawskiej, tak komentuje złożoność tego procesu:
„Fizyczna separacja U-235 od U-238 jest jednym z najbardziej wyrafinowanych osiągnięć inżynierii XX wieku. Pomimo postępu technologicznego, pozostaje to proces niezwykle energochłonny. To, że udało się to Związkowi Radzieckiemu w tak krótkim czasie po wojnie, świadczy o determinacji i ogromnych zasobach, jakie zostały zaangażowane, w tym o surowcu z Kowar.”
VI. Zastosowanie i dziedzictwo
Dziś, wiedząc o różnicy między U-235 a U-238, możemy docenić dziedzictwo Kowar. Wydobyty tu uran, choć naturalny i nisko skoncentrowany, był kluczowym surowcem wejściowym dla radzieckich zakładów wzbogacania. Bez niego program jądrowy ZSRR nie mógłby tak szybko ruszyć.
U-235 pozostaje fundamentem współczesnej energetyki, zasilając miliony domów na całym świecie jako nisko wzbogacone paliwo. Jednocześnie jego bliźniak, U-238, pełni rolę stabilizatora, jest bazą do produkcji plutonu i stanowi dominujący materiał w naturze.
Kowary dostarczyły U-235 dla globalnej historii. Zwiedzając Podziemną Trasę Turystyczną, pamiętajmy, że każda tona tej wydobytej rudy miała swój mały, ale strategiczny ułamek, który zadecydował o wejściu świata w Erę Atomu.